MEKANISME REAKSI OKSIDASI PADA SENYAWA ORGANIK
Reaksi oksidasi sendiri adalah pelepasan electron yang terjadi pada sebuah molekul, atom ataupun pada ion. Dalam artian dimana electron di hilangkan dan kerapatan suatu molekul berkurang. Oksidasi sendiri kebanyakan terjadi pada udara atau oksigen. Ada beberapa reaksi untuk oksidasi organic yaitu ;
-Transfer electron tunggal
-Oksidasi terjadi melalui zat antara ester dengan asam kromat ataupun mangan dioksida
-Oksidasi dimana ia melibatkan suatu reaksi eliminasi seperti oksidasi swern, oksidasi kornblum dan dengan reagen misalnya pada asam IBX dan periodinane Dess Martin
-Oksidasinya mengaitkan ozon dalam ozonolisis atau peroksida seperti asam peroksi
Reaksi oksidasi pada alkana
Reaksi oksidasi pada alkana dimana pada reaksi nya terdapat dua reaksi oksidasi yaitu reaksi oksidasi sempurna dan reaksi oksidasi tak sempurna.
Contoh :
Reaksi oksidasi sempurna
CH4 + 2O2 –a’ CO2 + 2H2O
Pada reaksi ini oksigen nya mencukupi
Reaksi oksidasi tak sempurna
CH4 + 2O2 –a’ CO + H2O
Dimana pada reaksi ini oksigennya tidak mencukupi
Reaksi oksidasi pada alkena
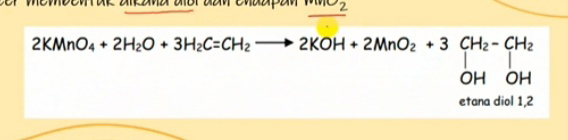
Reaksi oksidasi pada alkena bisa di oksidasi oleh suatu oksidator yaitu oleh KMnO4 karena ia bisa mengoksidasi alkena tapi oksidasi ini harus dilakukan dalam suasana asam maka ia bisa mengalami reaksi oksidasi membentuk alkana diol yaitu suatu senyawa alcohol yang memiliki dua gugus OH. Dan ia juga akan membentuk endapan MnO2. 2KMnO4 berperan sebagai oksidator maka alkena berubah mejadi alkana diol. Jadi pada alkena terjadi pemutusan ikatan rangkap menjadi berikatan dengan OH maka 2MnO2 menjadi endapan. Pada alkana diol terdapat dua OH yang berikatan dengan karbon yang berikatan rangkap tadi.
Bagaimana jika apa alkena digunakan oksidator yang kuat dalam proses oksidasinya maka ikatan rangkapnya akan pecah dan membentuk campuran asam, oksidator yang dimaksud adalah yang memiliki nilai potensial readuksi standar lebih besar, maka ia akan terbentuk campuran asam atau dikenal asam organic yaitu –COOH, sebelum terbentuk campuran asam ia mula-mula terbentuk aldehid terlebih dahulu. Dimana ikatan rangkap keduanya putus sehingga masing-masing karbon kekurangan dua tangan, dua tangan nya ini nanti akan berikatan dengan oksigen membentuk senyawa aldehid yaitu etanal dan propanal. Kemudian masing-masing senyawa teroksidasi kembali membentuk suatu asam organic dimana atom C nya tadi mengikat H jadi mengikat OH sehingga terbentuklah dua campuran asam.
Permasalahan :
1. Apa perbedaan yang mendasar antara reaksi oksidasi pada senyawa organic dengan senyawa anorganik ?
2. Pada reaksi alkena bagaimana jika ia di reaksikan dengan oksidator yang lemah, apa yang terjadi ?
3. Bagaimana perbedaan reaksi oksidasi sempurna dengan reaksi oksidasi tidak sempurna selain dari sisi oksigennya ? jelaskan !!




Baiklah saya Binro Naibaho dengan NIM A1C19049 akan menjawab permasalahan nomor 2. Nukleofilik bisa menyerang dari atas dan bawah maupun segala arah karena karbon dari aldehid/keton merupakan SP2 yang geometrinya planar yang dapat menempati bidang dari serangan manapun. Terimakasih
BalasHapusSaya Lara Prastica NIM A1C119045, ingin menjawab permasalahan no 3. Pada reaksi reagensia Grignard di lakukan hidrolisis dalam suasana asam bagaimana jika ia di hdrolisis dalam suasana basa ?
BalasHapusJawaban : menurut saya jika dalam suasana basa maka reaksi adisi alkohol ini tidak akan berjalan baik secara cepat ataupun lambat dan ini tidak bisa dilakukan dalam suasana basa. suasana asam disini berguna pada saat protonasi menekan muatan positif pada atom karbonil dan menjadikannya sasaran baik bagi serangan nukleofil (basa lemah).jika menggunakan suasana basa maka dia tidak bisa menekan muatan positif pada atom karbonil sehingga nukleofil tidak bisa menyerang dan tidak bisa terjadi reaksi adisi.
Saya Lara Prastica NIM A1C119045, ingin menjawab permasalahan no 3. Pada reaksi reagensia Grignard di lakukan hidrolisis dalam suasana asam bagaimana jika ia di hdrolisis dalam suasana basa ?
BalasHapusJawaban : menurut saya jika dalam suasana basa maka reaksi adisi alkohol ini tidak akan berjalan baik secara cepat ataupun lambat dan ini tidak bisa dilakukan dalam suasana basa. suasana asam disini berguna pada saat protonasi menekan muatan positif pada atom karbonil dan menjadikannya sasaran baik bagi serangan nukleofil (basa lemah).jika menggunakan suasana basa maka dia tidak bisa menekan muatan positif pada atom karbonil sehingga nukleofil tidak bisa menyerang dan tidak bisa terjadi reaksi adisi.